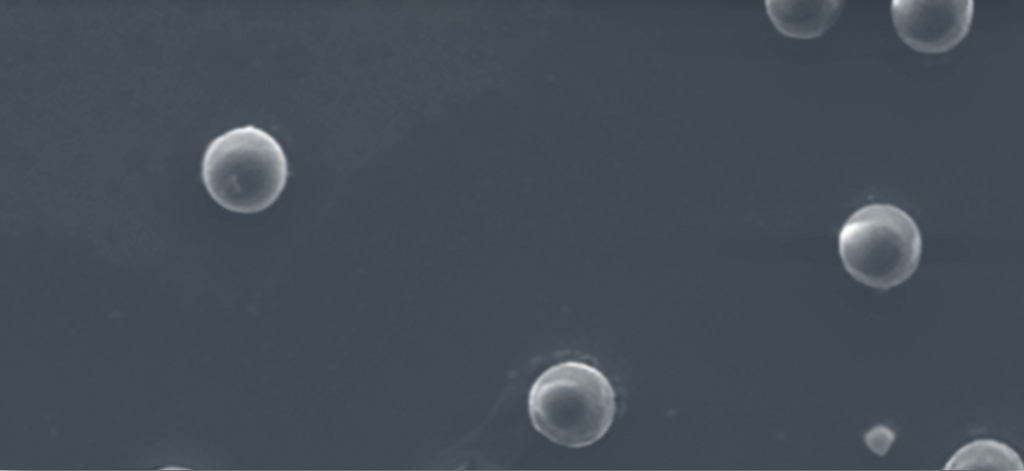
Con el propósito de dotar a la nanomedicina de una herramienta más para el tratamiento de diversas enfermedades, científicos del Centro de Investigación en Alimentación y Desarrollo (CIAD) crearon micro y nanoesferas capaces de liberar sustancias como la insulina para el control de pacientes diabéticos.
A cargo del doctor Agustín Rascón Chu, como parte del proyecto de investigación “Micro/nanoesferas basadas en pectinas de bajo metoxilo/arabinoxilanos ferulados como sistemas de liberación controlada de insulina”, se desarrolló el método para el diseño y fabricación automática de partículas acarreadoras que tienen un amplio campo de aplicación en la biomedicina.
En entrevista para la Agencia Informativa Conacyt, el doctor en Ciencia de los Alimentos por la École Nationale Supérieure Agronomique de Montpellier, en Francia, explicó el impacto de esta innovación financiada por el Fondo Institucional del Consejo Nacional de Ciencia y Tecnología (Conacyt) en 2012, en el que destaca el control en la talla y morfología de partículas en la meso y nanoescala que pueden alojar distintas moléculas de interés terapéutico.
Integrante del Sistema Nacional de Investigadores (SNI) nivel I, Rascón Chu detalló que este trabajo es complementario de otro en el que se estudia la liberación de insulina para administración oral, así como su eficacia in vivo, y que también se desarrolla en el CIAD, instancia que pertenece al Sistema de Centros Públicos de Investigación del Conacyt.

Dr. Agustín Rascón Chu
La investigación se desarrolló en el seno de la Red Temática de Nanociencias y Nanotecnología (Nanored) de Conacyt, y en ella participaron científicos del Centro de Investigación de Materiales Avanzados (Cimav), de la Universidad Autónoma de San Luis Potosí (UASLP) y de diversas coordinaciones del CIAD.
Agencia informativa Conacyt (AIC): ¿En qué consistió el proyecto?
Agustín Rascón Chu (ARCh): En este trabajo desarrollamos el método de fabricación de micro y nanoesferas con el propósito de resolver los problemas que se tienen con otros procedimientos. Uno de ellos es la dispersión de tamaños, porque en el análisis de la liberación de proteínas, vitaminas y otros compuestos de interés terapéutico eso nos causaba inconvenientes porque no podíamos tener un área constante de interacción entre la partícula y su medio, lo cual alteraba la liberación.
Fue así que nos dimos a la tarea de evaluar la técnica de electroaspersión y desarrollamos un método para la fabricación de las esferas, en el que, controlando las distintas condiciones, pudimos disminuir la dispersión de tamaños con la ventaja de que lo realizamos de manera automática.
AIC: ¿Con qué técnica realizan las esferas?
ARCh: El procedimiento que realizamos se basa en un movimiento electrohidrodinámico producido por la electroaspersión. Esta es una técnica del siglo XIX que fue descubierta al aplicar una carga sobre una solución, y ver que esa carga rompe la tensión superficial. Mediante la electroaspersión se generan micro y nanogotas y se basa en los mismos principios del electrospinning.
Con nuestro método podemos tener arreglo dentro de la esfera; lo que logramos fue generar núcleo y coraza. Tenemos núcleos donde hemos atrapado diversas moléculas modelo, tales como insulina, enzima pronasa, licopeno y también hemos atrapado probióticos.
AIC: ¿El aporte de su trabajo es el control del tamaño?
ARCh: En efecto. Anteriormente se fabricaban las esferas de forma manual con una jeringa, lo cual resultaba poco eficiente; entonces, mediante el equipamiento que logramos podemos ahora, de manera automática, fabricar y controlar la dispersión de tamaños.
Algo interesante de nuestro modelo es que no se trata de autoensamblaje, sino que podemos determinar un tamaño conveniente a las aplicaciones de interés. Mediante distintas condiciones es posible determinar el tamaño que queremos de la partícula, dejando atrás la distribución aleatoria de tallas.
Ahora se puede determinar si el tamaño conveniente es, por ejemplo, de una micra, y qué condiciones de fabricación resultan más propicias. De hecho, ya probamos esa medida para ser aplicada a condiciones de colon, como una parte complementaria a otro proyecto que era liberación dirigida a colon. En ese caso pensamos en tamaños de una micra y logramos tener partículas de 1 ± 0.24 micrómetros (µm) de diámetro, y eso nos abrió nuevas aplicaciones. Lo más pequeño que hemos obtenido es de hasta cuatro nanómetros; de ahí nos extendemos, tanto en la nanoescala como en la mesoescala.
AIC: ¿Cuáles serían las aplicaciones de este desarrollo?
ARCh: Estas micro y nanopartículas pueden tener distintas aplicaciones y en ese caso en específico era para liberación dirigida a colon; sin embargo, puede haber aplicaciones diversas. Hay proyectos relacionados donde son aplicados para la piel o a nivel intravenoso, pero eso ya depende de otras ideas que tengan los investigadores.
Por ejemplo, está pensada para pacientes diabéticos, en el caso de aplicar insulina, o apósitos en la piel para la gente con psoriasis. Debido a que hemos logrado atrapar diversas sustancias y por el material con que están hechas, podemos tener una amplia gama de aplicaciones, ya que las fibras que usamos tienen mucoadhesividad y biocompatibilidad ya probada.
AIC: ¿De qué están hechas?
ARCh: Las elaboramos con polímeros que provienen de paredes vegetales, que normalmente no tienen un valor comercial alto; algo que nos parece un gran aliciente es que a partir de residuos agrícolas y de la agroindustria podemos recuperar polisacáridos de alto valor agregado y darle una aplicación de alto impacto, como es la biomedicina.
Estos polímeros neutros en olor y sabor son parte de la dieta del mexicano, pectinas y arabinoxilanos que están en frutas e incluso en las tortillas de maíz. Estas fibras están reportadas como prebióticas y disminuyen el colesterol en la sangre; es decir, ya está reportado su efecto benéfico a la salud por sí mismas.
AIC: ¿A qué retos se enfrentaron en el transcurso de la investigación?
ARCh: Hubo muchos retos a lo largo del camino. Tuve la suerte de contar con muy buenos colaboradores y con estudiantes muy comprometidos. El mayor reto fue la importación del equipo porque CIAD no contaba con un electroaspersor, y afortunadamente pudimos tenerlo.
Otro reto fue el diseño de las agujas porque no existían aún en el mercado, por lo que un colaborador en el extranjero las diseñó específicamente para este equipo; ahora ya las fabrican a nivel comercial.
AIC: ¿Cuál será el siguiente paso?
ARCh: Estamos en el proceso de solicitar la patente en biomedicina, con la posibilidad de que hagamos la transferencia de tecnología, especialmente con los resultados de los proyectos complementarios.
Nuestro proyecto termina en el diseño y fabricación de la partícula, determinando el tamaño y morfología. Pero a la par se ha relacionado con proyectos para vehículos de liberación de fármacos dirigida a colon, en donde ya se llevó la prueba a nivel in vivo en modelo murino (probado en ratas), y dependiendo de los resultados de ese trabajo, que se vislumbran muy favorables, posiblemente haya interesados en la transferencia de tecnología.

Colaboración de Ana Luisa Guerrero /Agencia Informativa Conacyt







